IL-31の受容体結合を競合的に阻害、かゆみによる悪循環遮断で皮膚症状改善・QOL向上に期待
マルホ株式会社は8月8日、ヒト化抗ヒトIL-31受容体Aモノクローナル抗体「ミチーガ(R)皮下注用60㎎シリンジ(一般名:ネモリズマブ(遺伝子組換え))」について、「アトピー性皮膚炎に伴うそう痒(既存治療で効果不十分な場合に限る)」を効能・効果として発売したことを発表した。
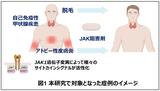
アトピー性皮膚炎は、増悪・軽快を繰り返す、かゆみのある湿疹を主病変とする慢性の炎症性皮膚疾患。アトピー性皮膚炎に伴うかゆみは、仕事や学業における集中力の低下や睡眠障害などを招き、患者のQOLを著しく低下させる。また、かゆみにより患部を引っかくことで皮膚症状が増悪し、さらにかゆみが強くなるという悪循環(イッチ・スクラッチサイクル)を引き起こす。現在、アトピー性皮膚炎のかゆみに対しては、抗炎症外用薬の併用のもと、抗ヒスタミン薬などが用いられるが、既存治療ではかゆみを十分にコントロールできない患者が存在する。このため、かゆみを標的とした新たな治療選択肢が求められている。
IL-31はかゆみを誘発するサイトカインであり、アトピー性皮膚炎に伴うかゆみの発生に関与していることが報告されている。ミチーガはIL-31とその受容体の結合を競合的に阻害し、アトピー性皮膚炎のかゆみに対する抑制作用を示す。かゆみによる悪循環を遮断することで皮膚症状も改善し、患者のQOLの向上が期待されている。用法・用量は、通常、成人及び13歳以上の小児にはネモリズマブ(遺伝子組換え)として1回60㎎を4週間の間隔で皮下投与することが示されている。
中外製薬創製、世界初のIL-31受容体A標的抗体医薬品
同剤は、中外製薬株式会社により創製されたIL-31受容体Aを標的とする世界で初めての抗体医薬品。マルホは、2016年9月に中外製薬と皮膚科疾患領域における国内ライセンス契約を締結後、同剤の開発を進め、2022年3月28日に製造販売承認を取得している。
マルホは、同剤の適正使用を通じて、アトピー性皮膚炎のかゆみに悩む患者のQOLの向上に貢献できるよう取り組んでいくとしている。(QLifePro編集部)